|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
ƒ^ƒ“ƒpƒNژ؟‚جگـ‚肽‚½‚ف”½‰ŒaکH‚ً’T‚é |
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
ƒ^ƒ“ƒpƒNژ؟‚ھƒ‰ƒ“ƒ_ƒ€ƒRƒCƒ‹‚جڈَ‘ش‚©‚çگ¶•¨‹@”\‚ًژ‚آچ\‘¢‚ةگ³‚µ‚گـ‚肽‚½‚ـ‚ê‚邱‚ئ‚ح”ٌڈي‚ة‘هگط‚بƒvƒچƒZƒX‚إ‚·پB‚»‚ê‚ھگ³‚µ‚چs‚ي‚ê‚ب‚¢‚½‚ك‚ة‹N‚«‚éڈd‘ه‚بژ¾ٹ³‚ھچإ‹ك‚¢‚‚آ‚©•ھ‚©‚ء‚ؤ‚«‚ؤژذ‰ï“I‚ب–â‘è‚ئ‚ب‚ء‚ؤ‚¢‚ـ‚·پBƒ^ƒ“ƒpƒNژ؟‚جƒ|ƒٹƒyƒvƒ`ƒhچ½‚ھ‚ظ‚ا‚¯‚é‚ئپA‚ئ‚肤‚éچ\‘¢‚جگ”‚ح“V•¶ٹw“I‚بگ”‚ة‚ب‚èپAˆê‚آˆê‚آ‚جچ\‘¢‚ًڈ„‚è•à‚¢‚ؤچإڈI‚ج“V‘Rچ\‘¢‚ة‚½‚ا‚è’…‚ٹm—¦‚حژہژ؟“I‚ة‚حƒ[ƒچ‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپAگـ‚肽‚½‚ف”½‰‚ة‚ح–¾ٹm‚ب”½‰ŒaکH‚ھ‘¶چف‚·‚é‚ئچl‚¦‚ç‚ê‚ؤ‚¢‚ـ‚·پB‚»‚ج”½‰ŒaکH‚ًŒˆ‚ك‚邱‚ئ‚ھپAƒQƒmƒ€ڈî•ٌ‚©‚çƒ^ƒ“ƒpƒNژ؟‹@”\‚ً’m‚邽‚ك‚ة‚àپAƒ^ƒ“ƒpƒNژ؟‚جچ\’zŒ´—‚ً’m‚邽‚ك‚ة‚àپA‚ـ‚½گـ‚肽‚½‚ف”½‰‚ًگ§Œن‚·‚邽‚ك‚ة‚à‘ه•دڈd—v‚إ‚·پBƒ^ƒ“ƒpƒNژ؟‚جگـ‚肽‚½‚ف–â‘è‚حپAXگüŒ‹ڈ»‰ًگح‚إƒ^ƒ“ƒpƒNژ؟‚ج—§‘جچ\‘¢‚ھڈ‰‚ك‚ؤ‰ً–¾‚³‚ꂽ“–ڈ‰‚©‚çٹw–â“I‚ة‚ح‹»–،‚ ‚é–â‘è‚ئ‚µ‚ؤ’چ–ع‚³‚ê‚ؤ‚«‚ـ‚µ‚½‚ھپAژہŒ±“I‚ة‚àپA—ک_“I‚ة‚à‰ً‚‚±‚ئ‚ھ”ٌڈي‚ة“‚¢–â‘è‚ئ‚µ‚ؤ–¢‰ً–¾‚ج‚ـ‚ـ40”N‹ك‚‚½‚ء‚ؤ‚¢‚ـ‚·پB |
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
ƒAƒ“ƒtƒHپ[ƒ‹ƒfƒBƒ“ƒO”½‰‚ج•ھژq“®—حٹwƒVƒ~ƒ…ƒŒپ[ƒVƒ‡ƒ“
پ@پ@ƒٹƒ]ƒ`پ[ƒ€‚جگـ‚肽‚½‚ف”½‰‚ًŒvژZ‹@ژہŒ±‚ة‚و‚ء‚ؤ’اگص‚·‚邱‚ئ‚حŒ»چف‚ج‚ئ‚±‚ë•s‰آ”\‚ب‚ج‚إپAˆب‰؛‚إ‚ح“V‘R—§‘جچ\‘¢‚ً‚ظ‚ا‚‚±‚ئ‚ًژژ‚ف‚ؤ‚ف‚ـ‚µ‚½پB•ھژq“à‚ة‘¶چف‚·‚éˆê–{‚جS-SŒ‹چ‡‚ًŒ‡‘¹‚³‚¹‚½3SS•دˆظ‘ج‚ًˆظڈي‚بچ‚‰·‚ة‚µ‚ؤ—§‘جچ\‘¢‚ً‰َ‚µ‚ؤ‚ف‚ـ‚µ‚½پB‚à‚؟‚ë‚ٌƒ^ƒ“ƒpƒNژ؟‚حگ…•ھژq‚ة”ي‚ي‚ê‚ؤ‚¢‚ـ‚·‚ھپA‚»‚ê‚حڈب—ھ‚µ‚ؤژهچ½‚جƒٹƒ{ƒ“–حŒ^‚إ•\ژ¦‚³‚ê‚ؤ‚¢‚ـ‚·پBƒ^ƒ“ƒpƒNژ؟‚ھ‰َ‚ê‚ؤ‚¢‚‰ك’ِ‚جƒXƒiƒbƒvƒVƒ‡ƒbƒg‚إ‚·‚ھپAژہŒ±“Iڈط‹’‚ح‚ـ‚¾ڈ\•ھ‚إ‚ح‚ ‚è‚ـ‚¹‚ٌپB |
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
چ¶‚جگ}‚حƒٹƒ]ƒ`پ[ƒ€‚ج“V‘R—§‘جچ\‘¢‚إ‚·پBچ¶’[‚جˆê–{‚جS-SŒ‹چ‡پi‰©گFپj‚ھگط’f‚³‚ꂽ3SS•دˆظ‘ج‚إ‚·پB“V‘R—§‘جچ\‘¢‚إ‚حگش‚¢‚S–{‚ج‚ضƒٹƒbƒNƒX‚©‚çگ¬‚éƒ؟ ƒhƒپƒCƒ“‚ئپA‚R–{‚جگآ‚¢ƒہƒXƒgƒ‰ƒ“ƒh‚©‚çگ¬‚éƒہƒhƒپƒCƒ“‚ھٹm”F‚إ‚«‚ـ‚·پB |
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
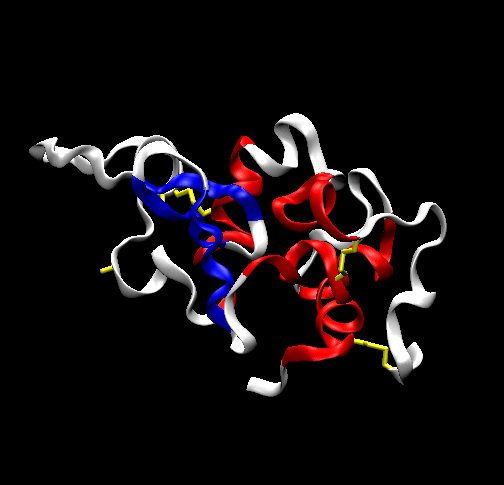 |
 |
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
‰E‚جگ}‚ح•ھژqچ¶‘¤‚جƒہƒhƒپƒCƒ“‚ھ‰َ‚êژn‚ك‚½‚±‚ئ‚ًژ¦‚µ‚ؤ‚¢‚ـ‚·پBƒہƒVپ[ƒg‚جƒgƒ|ƒچƒWپ[‚ح‚ـ‚¾ژc‚ء‚ؤ‚¢‚ـ‚·‚ھŒ`‚ح•ِ‚ê‚ؤ‚¢‚ـ‚·پBˆê•ûپA•ھژq‰E‘¤‚جƒ؟ƒhƒپƒCƒ“‚ج‚ضƒٹƒbƒNƒX‚حڈ‚µکc‚ٌ‚إ‚¢‚é‚à‚ج‚ج“V‘Rچ\‘¢‚ھ•غ‘¶‚³‚ê‚ؤ‚¢‚ـ‚·پB |
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
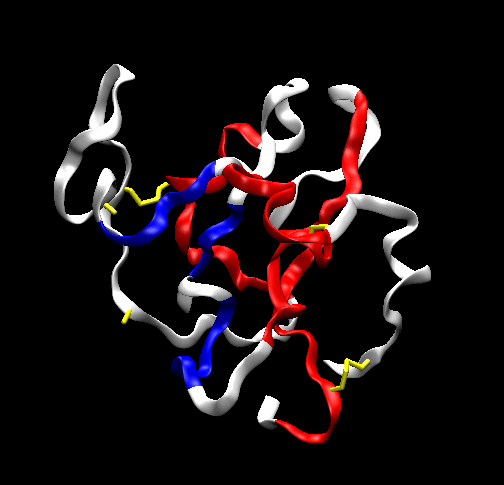 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
چ¶‚جگ}‚إ‚حپA‚³‚ç‚ةچ½‚ھ‚ظ‚ا‚¯‚ؤ‚ضƒٹƒbƒNƒX‚àڈءژ¸‚µ‚ؤ‚¢‚ـ‚·پBS-SŒ‹چ‡‚ھ‘¶چف‚µ‚ؤ‚¢‚邽‚كچ½‚جƒgƒ|ƒچƒWپ[‚ح•غ‘¶‚³‚ê‚ؤ‚¢‚ـ‚·‚ھپAچ½‚جٹe•”•ھ‚حƒ‰ƒ“ƒ_ƒ€ƒRƒCƒ‹ڈَ‚ة‚ب‚ء‚ؤ‚¢‚ـ‚·پB‹»–،‚ ‚邱‚ئ‚ةپAژهچ½‚ھƒ^پ[ƒ“‚µ‚ؤگـ‚ê‹ب‚ھ‚é—جˆو‚ھ•غ‘¶‚³‚ê‚ؤ‚¢‚é‚و‚¤‚ةŒ©‚¦‚ـ‚·پB |
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
ƒ~ƒXƒtƒHپ[ƒ‹ƒfƒBƒ“ƒO•aپ@پiƒRƒ“ƒtƒHƒپپ[ƒVƒ‡ƒ“•aپj
پ@پ@‚½‚ء‚½ˆê‚آ‚جƒAƒ~ƒmژ_’uٹ·‚ھ‚¨‚«‚ؤƒ^ƒ“ƒpƒNژ؟‚جگ³‚µ‚¢—§‘جچ\‘¢‚ھŒ`گ¬‚إ‚«‚ب‚¢‚½‚ك‚ة‹N‚«‚éˆâ“`“Iژ¾ٹ³‚à‚ ‚è‚ـ‚·‚ھپAچإ‹ك‚حƒAƒ~ƒmژ_’uٹ·‚ھ‹N‚«‚ب‚‚ؤ‚à•¨—“I‚ب—§‘جچ\‘¢‚ھٹشˆل‚ء‚ؤ‚¢‚邽‚ك‚ة‹N‚«‚éƒAƒ~ƒچƒCƒhژ¾ٹ³‚ب‚ا‚ھ‚و‚’m‚ç‚ê‚ؤ‚¢‚ـ‚·پBƒvƒٹƒIƒ“•a‚ئŒؤ‚خ‚ê‚éگ_Œoژ¾ٹ³‚àƒvƒٹƒIƒ“ƒ^ƒ“ƒpƒNژ؟‚جƒ؟‚ضƒٹƒbƒNƒX‚ھƒہƒVپ[ƒg‚ة“]ٹ·‚³‚ê‚邱‚ئ‚ة‚و‚ء‚ؤ‹N‚«‚é‚ئچl‚¦‚ç‚ê‚ؤ‚¢‚ـ‚·پB |
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
|
|
 |
|
 |
|
|
|
|
|
|
|
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |


